A maioria dos gestores de varejo de saúde que evita fazer marketing nas redes sociais ou em anúncios digitais usa a mesma justificativa: “tem muita restrição da Anvisa, é arriscado, prefiro não fazer.” Essa prudência tem uma base real, mas está sendo aplicada de forma excessivamente ampla e está custando oportunidades de comunicação que são completamente legais.
A RDC 96/2008 da Anvisa, a Resolução da Diretoria Colegiada que regula a publicidade de medicamentos no Brasil, é uma norma sobre um objeto muito específico: a propaganda de medicamentos. Não é uma norma sobre marketing de varejo farmacêutico, não é uma norma sobre comunicação de estabelecimentos de saúde e não é uma norma sobre publicidade de serviços ou de categorias de produto que não são medicamentos.
O gestor que entende a diferença entre o que a norma restringe e o que ela não menciona tem acesso a um espaço de comunicação muito maior do que imagina. A RDC 96 não proíbe o marketing do varejo de saúde. Ela proíbe determinadas práticas de propaganda de medicamentos. E essa distinção muda completamente o que o gestor pode e não pode fazer.
Este artigo apresenta, com precisão e sem alarmismo, o que a norma restringe, o que ela permite explicitamente e onde está o espaço de comunicação que a maioria dos estabelecimentos independentes ainda não explora por desconhecimento da legislação.
O que é a RDC 96/2008 da Anvisa e a quem ela se aplica
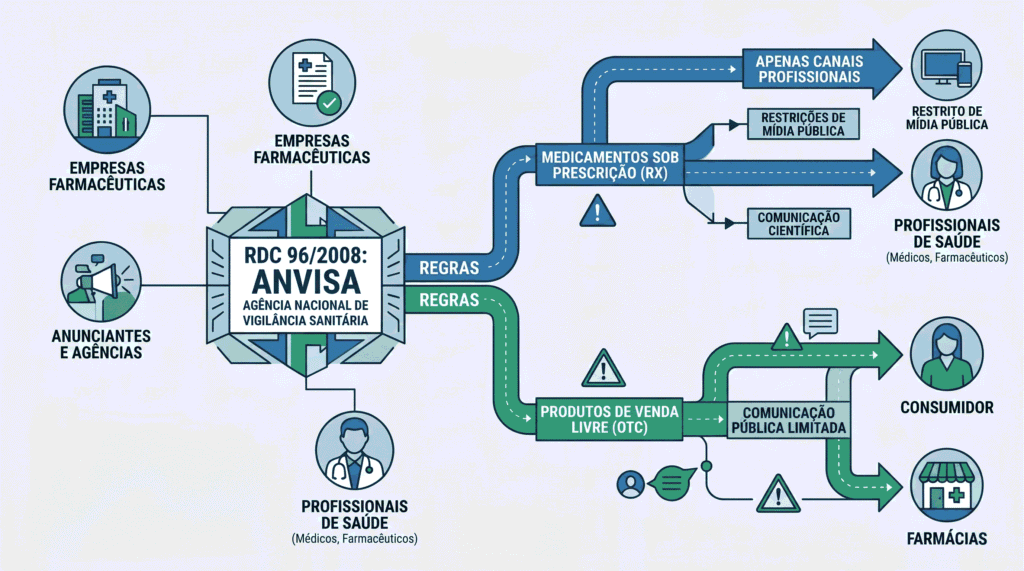
A RDC 96/2008 é a resolução da Agência Nacional de Vigilância Sanitária que dispõe sobre a propaganda, publicidade, informação e outras práticas cujo objetivo seja a divulgação ou promoção comercial de medicamentos.
Ela se aplica primariamente a fabricantes, distribuidores, importadores e outras entidades da cadeia de produção e distribuição de medicamentos que realizam propaganda do produto em si. O seu foco regulatório é a propaganda do medicamento enquanto produto: a promoção de um princípio ativo específico, de uma marca comercial de medicamento, de uma indicação terapêutica.
A norma não regula, de forma específica e primária, a comunicação de um estabelecimento farmacêutico sobre os serviços que oferece, sobre as categorias de produto disponíveis em geral, sobre sua identidade de marca ou sobre o atendimento que presta. Esses elementos estão sujeitos às normas gerais de publicidade do CONAR e às diretrizes do Conselho Federal de Farmácia, mas não ao escopo central da RDC 96.
Essa distinção é fundamental: há diferença entre anunciar um medicamento específico com indicação terapêutica (sujeito à RDC 96) e comunicar que um estabelecimento de saúde tem amplo estoque, entrega rápida e atendimento farmacêutico especializado (não sujeito ao escopo central da RDC 96).
O que a RDC 96 proíbe de forma expressa
A norma lista de forma específica as práticas vedadas na propaganda de medicamentos. Conhecer essas vedações é o ponto de partida para entender onde estão os limites reais.
Propaganda de medicamentos de venda sob prescrição para o público leigo
Medicamentos que exigem receita médica, os chamados medicamentos éticos, não podem ter propaganda direcionada ao consumidor final. Isso inclui antibióticos, ansiolíticos, antidepressivos, anti-hipertensivos, hipoglicemiantes, entre outros. A propaganda desses medicamentos é restrita a profissionais de saúde habilitados.
O que isso significa na prática para o varejo de saúde: um post no Instagram mostrando o produto Zolpidem (medicamento para insônia) com a indicação “para quem tem dificuldade de dormir, peça agora pelo WhatsApp” viola a RDC 96. A propaganda direta de um medicamento de prescrição para o consumidor é vedada independentemente do canal.
Afirmações que atribuem propriedades terapêuticas não comprovadas
A norma proíbe que qualquer material publicitário atribua a um medicamento propriedades terapêuticas que não estejam registradas na bula aprovada pela Anvisa ou que não tenham embasamento científico reconhecido. Promessas como “elimina a doença”, “garante a cura” ou “trata definitivamente” são vedadas mesmo para medicamentos de venda livre.
O que isso significa na prática: comunicar que determinado produto “alivia os sintomas de gripe” é usar a indicação registrada. Comunicar que “cura a gripe em 24 horas” é uma afirmação não comprovada que viola a norma.
Uso de profissionais de saúde como endossantes de medicamentos específicos
A RDC 96 veda o uso de imagem ou depoimento de profissionais de saúde (médicos, farmacêuticos, nutricionistas) para recomendar ou endossar medicamentos específicos em propaganda direcionada ao público leigo. O profissional de saúde pode ser mostrado em contexto de cuidado, mas não pode aparecer recomendando um medicamento específico.
O que isso significa na prática: um farmacêutico apresentando um vídeo sobre cuidados com a saúde cardiovascular não viola a norma. O mesmo farmacêutico dizendo “eu recomendo o [marca de medicamento] para pressão alta” em um post de rede social viola.
Indução ao consumo desnecessário de medicamentos
A norma proíbe práticas publicitárias que induzam o consumo de medicamentos sem necessidade terapêutica identificada, especialmente aquelas que associam o uso do medicamento a situações de bem-estar, de produtividade ou de performance social sem relação com uma condição de saúde específica.
O que isso significa na prática: comunicar que o paracetamol está disponível para quando surgir febre ou dor é informação contextualizada em condição de saúde. Comunicar que “tome nosso analgésico para aguentar o dia de trabalho” é indução a consumo sem indicação terapêutica clara.
Uso de imagens que associem medicamentos a felicidade, status ou sucesso
A norma veda o uso de imagens, personagens ou narrativas que associem o uso de medicamentos a estados emocionais positivos desvinculados da condição de saúde tratada, como felicidade, sucesso profissional, beleza ou popularidade.
O que isso significa na prática: mostrar uma pessoa sorrindo após se recuperar de uma gripe com o uso de um medicamento é aceitável. Mostrar uma pessoa “mais feliz e bem-sucedida” porque toma determinado suplemento medicamentoso é associação vedada.
O que a RDC 96 permite, e o que a norma não regula
Este é o lado da norma que a maioria dos gestores de varejo de saúde desconhece, e onde está o maior espaço de oportunidade para comunicação legítima e eficaz.
Propaganda de medicamentos isentos de prescrição com alegações dentro da bula
Medicamentos de venda livre, denominados MIPs (Medicamentos Isentos de Prescrição), podem ser anunciados para o público leigo desde que as alegações utilizadas estejam dentro das indicações registradas na bula aprovada pela Anvisa.
Isso inclui: antitérmicos, analgésicos, antidiscos, antigripais, antiácidos, laxativos, vitaminas e minerais sem indicação de tratamento de doença específica, entre outros. Um estabelecimento de saúde pode comunicar a disponibilidade desses produtos, destacar o preço e informar a indicação aprovada pela bula sem violar a norma.
O volume de MIPs disponíveis no mercado brasileiro é expressivo. Comunicá-los com indicação de uso dentro da bula é uma estratégia de marketing legítima e de alto potencial de conversão por exatamente porque são os produtos mais buscados pelos consumidores em momento de necessidade.
Comunicação institucional e de identidade do estabelecimento
A RDC 96 não restringe a comunicação de um estabelecimento de saúde sobre sua identidade, seus diferenciais de atendimento, sua localização, seus horários, seus serviços e sua proposta de valor. Comunicar que o estabelecimento tem atendimento farmacêutico especializado, delivery em 45 minutos, estoque completo de medicamentos e equipe treinada não é propaganda de medicamento. É marketing de serviço.
Esse espaço é amplíssimo e quase completamente inexplorado pela maioria dos estabelecimentos independentes, exatamente porque o gestor confunde a restrição de propaganda de medicamento com restrição de marketing do estabelecimento. São objetos completamente diferentes.
Conteúdo educativo sobre saúde e prevenção
Publicar conteúdo educativo sobre condições de saúde, hábitos preventivos, orientações gerais de bem-estar e cuidados com a saúde é não apenas permitido como é encorajado pelo Conselho Federal de Farmácia como exercício da atenção farmacêutica.
Um vídeo explicando a diferença entre gripas viral e bacteriana, os cuidados gerais com a saúde cardiovascular, a importância da adesão ao tratamento de diabetes ou os benefícios da suplementação de vitamina D para determinados perfis de paciente não viola nenhuma norma. Esse tipo de conteúdo constrói autoridade, gera alcance orgânico e posiciona o estabelecimento como referência de orientação de saúde na comunidade.
Promoção de suplementos e produtos de saúde preventiva com alegações funcionais aprovadas
Suplementos alimentares, vitaminas, minerais, probióticos e outros produtos de saúde preventiva têm alegações funcionais aprovadas pela Anvisa que podem ser usadas em comunicação publicitária. “Vitamina C contribui para o funcionamento normal do sistema imune” é uma alegação funcional aprovada. “Probióticos contribuem para o equilíbrio da flora intestinal” também é.
Essas categorias de produto têm crescimento de 31% ao ano no varejo farmacêutico brasileiro e margem entre 35% e 65%, segundo dados do IQVIA e da ABIAD. Comunicá-las com as alegações funcionais aprovadas é uma das estratégias de marketing de maior retorno disponível para o varejo de saúde independente, dentro de uma estrutura completamente legal.
Como aprofundamos no artigo Saúde preventiva como oportunidade de receita: como o movimento de wellness está criando uma nova categoria de demanda no balcão, a comunicação de wellness dentro da regulação não exige abandono da persuasão. Exige precisão de linguagem, e essa precisão, quando dominada, transforma a restrição em diferencial de credibilidade.
Comunicação de preço e de disponibilidade de produto
Publicar o preço de um medicamento de venda livre disponível em estoque, comunicar a chegada de um produto e informar a disponibilidade de apresentações específicas são ações de comunicação comercial que não se enquadram no escopo de propaganda regulada pela RDC 96. Encarte de oferta com produtos MIPs com preço, apresentação e condição de compra é uma forma de comunicação legítima e de alto impacto de conversão.
O encarte farmacêutico, seja em formato impresso ou digital distribuído pelo WhatsApp e redes sociais, comunica disponibilidade e preço de produto, não propaga indicação terapêutica de medicamento. Essa distinção é relevante e protege o estabelecimento dentro de uma estratégia de comunicação bem estruturada.
A linha que separa o permitido do proibido: guia prático
Para o gestor que precisa de uma referência operacional clara, a diferença entre comunicação permitida e comunicação vedada pode ser resumida em uma pergunta central:
“Esta comunicação está promovendo um medicamento específico (marca ou princípio ativo) com indicação terapêutica para o público leigo, ou está promovendo o estabelecimento, um serviço, uma categoria de produto ou um produto não medicamentoso?”
Se a resposta for a segunda opção, a comunicação não está no escopo central da RDC 96 e pode ser realizada com as diretrizes gerais de publicidade do CONAR como referência, que são consideravelmente mais permissivas.
Exemplos comparativos, Não permitido versus Permitido:
- Não permitido: “Losartana 50mg: para controlar sua pressão, peça agora”: propaganda de medicamento de prescrição com indicação terapêutica para o público leigo.
- Permitido: “Precisa de medicamentos para uso contínuo? Temos estoque completo e entrega rápida. Consulte nossa disponibilidade pelo WhatsApp”: comunicação de serviço do estabelecimento sem propaganda de medicamento específico.
- Não permitido: “Nossa vitamina D cura deficiência imunológica”: promessa terapêutica não comprovada e não registrada.
- Permitido: “Vitamina D 2.000 UI: contribui para o funcionamento normal do sistema imune. Disponível em cápsulas. Peça pelo WhatsApp.”: alegação funcional aprovada pela Anvisa para suplemento vitamínico.
- Não permitido: “Dr. [Nome], médico cardiologista, recomenda nosso ômega-3 para saúde do coração”: endosso de profissional de saúde a medicamento/suplemento específico vedado pela norma.
- Permitido: “Nossa equipe farmacêutica está disponível para orientar sobre suplementação cardiovascular. Agende uma consulta gratuita.”: comunicação de serviço de atenção farmacêutica sem endosso a produto específico.
- Não permitido: “Antibiótico sem receita, entrega em 40 minutos”: anúncio de medicamento de prescrição para público leigo e incentivo à automedicação com produto de venda controlada.
- Permitido: “Drogaria com entrega em 40 minutos. Aceitamos receitas digitais e físicas. Faça seu pedido pelo WhatsApp.”: comunicação de serviço de delivery sem referência a medicamento de prescrição específico.
O papel do Conselho Federal de Farmácia na regulação da comunicação do farmacêutico
Além da RDC 96, o farmacêutico responsável técnico está sujeito às diretrizes do Conselho Federal de Farmácia (CFF) e do Conselho Regional de Farmácia (CRF) de cada estado, que regulam o exercício da atenção farmacêutica e a comunicação do profissional de saúde.
As principais orientações do CFF para a comunicação do farmacêutico em redes sociais e em outras plataformas digitais incluem:
- O farmacêutico pode publicar conteúdo educativo sobre saúde, medicamentos e prevenção, desde que não faça indicação terapêutica específica para um paciente não avaliado.
- O farmacêutico pode orientar sobre o uso correto de medicamentos de venda livre e sobre suplementos com alegações funcionais aprovadas.
- O farmacêutico não deve fazer diagnóstico remoto nem indicar medicamentos de prescrição sem avaliação clínica presencial ou por teleconsulta regulamentada.
- O uso da imagem do farmacêutico em comunicação do estabelecimento está permitido desde que não configure endosso a produto específico de forma que induza a automedicação.
Essas diretrizes, somadas ao escopo da RDC 96, definem um espaço de comunicação farmacêutica legítima que é muito mais amplo do que a maioria dos gestores e farmacêuticos percebe. O medo de violar a norma está coibindo comunicação que está completamente dentro da legalidade.
Como a restrição regulatória pode se tornar diferencial competitivo
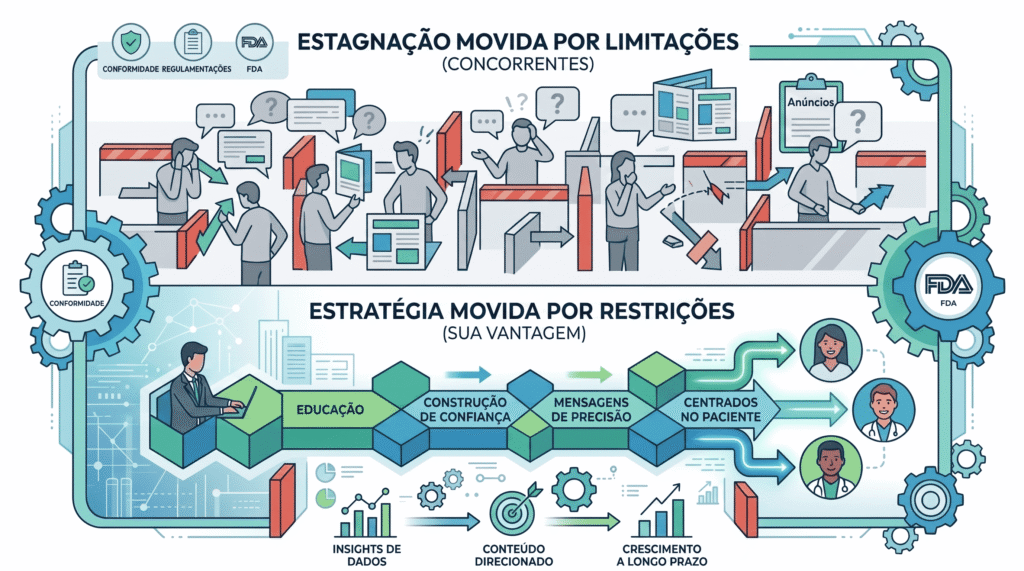
Existe uma leitura estratégica da regulação de publicidade farmacêutica que poucos gestores fazem: as restrições que se aplicam ao setor se aplicam igualmente a todos os concorrentes. O gestor que domina o que pode ser comunicado dentro da norma tem vantagem competitiva sobre o concorrente que ou viola a norma por desconhecimento (e se expõe a autuação) ou deixa de comunicar por medo excessivo (e perde oportunidade de conversão).
Dominar a regulação não é apenas proteção legal. É diferencial de comunicação. Um estabelecimento que comunica com precisão de linguagem, dentro das alegações aprovadas, demonstra para o paciente um nível de profissionalismo e de cuidado que distingue a operação de qualquer concorrente que comunica de forma genérica ou que não comunica.
O paciente que recebe informação correta, dentro do escopo aprovado, com linguagem acessível e orientação qualificada, percebe um nível de cuidado que constrói mais confiança do que qualquer promessa extravagante. A regulação, quando entendida e aplicada corretamente, não limita o marketing do varejo de saúde. Ela define o padrão de excelência da comunicação.
Como discutimos no artigo Redes sociais geram alcance. O que converte esse alcance em receita para o seu estabelecimento, a estrutura de conversão de redes sociais para o varejo de saúde opera de forma mais eficiente quando o conteúdo é construído com precisão regulatória, porque isso elimina o risco de reprovação por parte das plataformas e constrói a autoridade que sustenta a taxa de conversão ao longo do tempo.
Perguntas frequentes sobre a RDC 96 e publicidade no varejo de saúde
O que é a RDC 96 da Anvisa?
A RDC 96/2008 é a Resolução da Diretoria Colegiada da Agência Nacional de Vigilância Sanitária que regula a propaganda, publicidade, informação e outras práticas de divulgação ou promoção comercial de medicamentos no Brasil. Ela estabelece o que pode e o que não pode ser comunicado sobre medicamentos em qualquer canal de comunicação, seja impresso, digital ou audiovisual. A norma se aplica primariamente à propaganda do medicamento enquanto produto e não regula de forma específica a comunicação institucional de estabelecimentos farmacêuticos sobre seus serviços, diferenciais e categorias de produto em geral.
Uma farmácia pode fazer anúncio de medicamento no Google ou no Instagram?
Depende do tipo de medicamento e da forma de comunicação. Medicamentos de venda livre (MIPs) podem ser anunciados para o público leigo desde que as alegações utilizadas estejam dentro das indicações registradas na bula aprovada pela Anvisa e que não haja promessas terapêuticas não comprovadas. Medicamentos de venda sob prescrição não podem ser anunciados para o público leigo em nenhum canal. Além da RDC 96, o Google e o Meta têm políticas próprias de publicidade para produtos de saúde que podem ser mais restritivas do que a norma brasileira, exigindo certificação específica para determinadas categorias de anúncio.
Quais categorias de produto o varejo de saúde pode comunicar sem restrição da RDC 96?
As categorias de produto e de comunicação que não estão no escopo central de restrição da RDC 96 incluem: suplementos alimentares e vitaminas com alegações funcionais aprovadas pela Anvisa, dermocosméticos e produtos de cuidado pessoal, serviços farmacêuticos (aferição de pressão, aplicação de injetáveis, orientação farmacêutica), produtos de higiene, comunicação institucional do estabelecimento (horários, localização, diferenciais de atendimento, delivery), conteúdo educativo sobre saúde e prevenção dentro das competências do farmacêutico, e preço e disponibilidade de MIPs sem alegação terapêutica que ultrapasse a bula registrada.
O que acontece se um estabelecimento violar a RDC 96?
A Anvisa pode aplicar sanções que variam desde advertência e multa até interdição do estabelecimento, cancelamento do registro do produto anunciado em desconformidade e proibição de distribuição. Os valores de multa previstos na Lei 6.437/1977, que regulamenta as infrações sanitárias, vão de R$ 2.000 a R$ 1,5 milhão por infração, dependendo da gravidade e da reincidência. Além das sanções da Anvisa, o Conselho Regional de Farmácia pode instaurar processo ético-disciplinar contra o farmacêutico responsável técnico pelo estabelecimento em casos de violação relacionada ao exercício profissional.
Farmácia pode fazer live ou Reels com farmacêutico orientando sobre saúde?
Sim, dentro do escopo de atenção farmacêutica. O farmacêutico pode publicar conteúdo em vídeo sobre saúde, prevenção, uso correto de medicamentos de venda livre, orientações gerais sobre condições de saúde e benefícios de suplementos com alegações funcionais aprovadas. O que não pode: fazer indicação terapêutica de medicamento de prescrição para o público leigo, recomendar nominalmente um medicamento específico de prescrição como tratamento para uma condição, ou fazer diagnóstico remoto de condição de saúde. Dentro desses limites, o conteúdo de vídeo com farmacêutico é uma das formas de comunicação de maior alcance e de maior autoridade disponíveis para o varejo de saúde.
A RDC 96 da Anvisa não é o motivo pelo qual o varejo de saúde independente comunica pouco. É a justificativa que o varejo usa para não comunicar o que poderia. O espaço de comunicação legítima disponível para um estabelecimento de saúde que domina a norma é amplo: suplementos, dermocosméticos, serviços farmacêuticos, conteúdo educativo, comunicação institucional, preço e disponibilidade de produtos de venda livre. Tudo isso pode ser comunicado com eficácia, com frequência e com retorno mensurável. O gestor que conhece esse espaço para de usar a regulação como desculpa e começa a usá-la como vantagem.
Agora que você sabe o que pode comunicar, o próximo passo é comunicar com consistência e com alcance.
A Symbol oferece duas soluções para transformar o espaço regulatório em resultado comercial:
Encarte Farma: comunicação de oferta semanal dentro da norma O Encarte Farma foi desenvolvido para o varejo de saúde com templates que comunicam produto, preço e disponibilidade dentro do escopo permitido pela regulação. Não há risco de alegação terapêutica inadequada nos modelos prontos. O gestor comunica com consistência semanal, sem designer e sem risco regulatório.
Pharma ADS: anúncios digitais construídos dentro das políticas de saúde do Google e do Meta O Pharma ADS opera com conhecimento prévio das restrições de publicidade de saúde das plataformas e da RDC 96. Os anúncios são configurados para maximizar conversão dentro do espaço regulatório permitido, sem reprovação e sem risco de autuação. A especialização no setor é o que diferencia uma campanha que funciona de uma campanha que viola a norma sem o gestor saber.
Comunicar dentro da norma com consistência e com alcance. Esse é o padrão da operação que cresce sem risco.
Conheça as soluções Symbol para comunicação regulada no varejo de saúde: